2015
年修订的《食品安全法》实施,保健食品行业迎来新变革,正式开启注册与备案分类管理新模式,此后,随着《保健食品注册与备案管理办法》、《保健食品备案工作指南》、
《保健食品原料目录与保健功能目录管理办法》
等配套文件的出台实施,“双轨制”下保健食品注册与备案工作正式拉开帷幕。
而今年3月1日,辅酶Q10等五种保健食品原料目录的正式实施,标志着功能类保健食品原料产品备案工作正式启动,保健食品备案产品不再局限是维生素和矿物质类原料。
保健食品实施备案管理后大大缩短了之前的注册时间,降低了企业成本,更利于企业经营和产品创新。而
未来,随着保健食品原辅料目录的不断扩充,更多天然植物提取物的原料将加入备案目录,保健食品备案类产品将越来越多。
哪些保健食品可以实行备案制?保健食品备案流程如何?申报要点、提交材料有哪些等等?下面龙八国际下载安装来逐一介绍。
一、
哪些保健食品可以备案
依照《保健食品注册与备案管理办法》,生产和进口下列保健食品应当依法备案:
1.
使用的原料已经列入保健食品原料目录的保健食品;
2.
首次进口的属于补充维生素、矿物质等营养物质的保健食品。
首次进口的属于补充维生素、矿物质等营养物质的保健食品,其营养物质应当是列入保健食品原料目录的物质。
划重点:
以辅酶Q10等五种原料为原料的备案仅针对国产保健食品,不包括首次进口的保健食品。
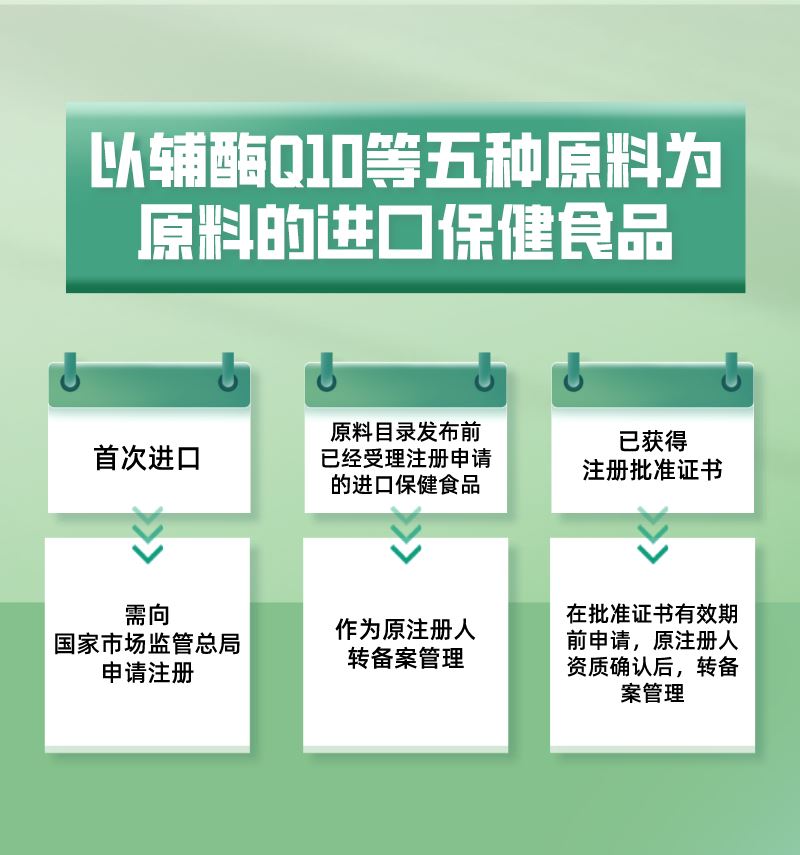
以辅酶Q10等五种原料为原料的进口保健食品目前监管如下方式进行:
二、
保健食品备案主体
1.
国产保健食品
国产保健食品备案人应当是保健食品生产企业,保健食品原注册人可以作为备案人。
原注册人包括:
(1)
《保健食品原料目录》发布前
受理的
保健食品注册申请,其原料已列入原料目录,且符合备案相关技术要求的,申请该产品备案的原注册申请人;
(2)
获得注册的保健食品,其原料已列入《保健食品原料目录》,且符合备案相关技术要求的,申请该产品备案的原注册人;
(3)
《保健食品原料目录》发布前受理的保健食品注册申请,以及获得注册的保健食品,其原料或用量不完全符合《保健食品原料目录》以及备案技术要求的,注册申请人或证书持有人同意按照《保健食品原料目录》调整产品原料和产品技术要求的,也可以作为原注册人。
但是,《保健食品原料目录》发布后受理的注册申请保健食品,其原料已列入《保健食品原料目录》,且产品符合相关技术要求,原注册申请人不可以作为原注册人申请该产品备案。
2.
进口保健食品
进口保健食品的备案人,应当是上市保健食品境外生产厂商。
三、
保健食品备案相关法律法规
|
序号
|
名称
|
发布日期
|
施行日期
|
|
1
|
*人民共和国食品安全法(2018年修订版)
|
2018.12.29
|
2018.12.29
|
|
2
|
保健食品注册与备案管理办法(2020年修订版)
|
2020.11.03
|
2020.11.03
|
|
3
|
保健食品备案工作指南(试行)
|
2017.05.02
|
2017.05.02
|
|
4
|
保健食品标注警示用语指南
|
2019.06.10
|
2019.08.20
|
|
5
|
保健食品命名指南(2019年版)
|
2019.11.10
|
2019.11.12
|
|
6
|
保健食品原料目录-营养素补充剂(2020年版)
|
2020.12.01
|
2021.03.01
|
|
7
|
辅酶Q10等五种保健食品原料目录
|
2020.12.01
|
2021.03.01
|
|
8
|
辅酶Q10等五种保健食品原料备案产品剂型及技术要求
|
2021.01.29
|
2021.06.01
|
|
9
|
保健食品备案产品可用辅料及其使用规定(2021年版)
|
2021.02.20
|
2021.06.01
|
|
10
|
保健食品备案产品剂型及技术要求(2021年版)
|
2021.02.20
|
2021.06.01
|
四、
保健食品备案流程及所需材料

龙八国际下载安装
(华微检测)
为广州市微生物研究所、广东华南新药创制中心及高水平技术团队共建的专门从事生物安全、生物医药及保健品等领域的第三方检测机构。华微检测实验室严格遵照ISO/IEC17025、RB/T214等标准、规范要求运行,并已取得第三方检测机构相关认证证书,在保健食品领域,可为客户提供从原料到产品、从注册备案咨询到代理申报、从动物毒理检测到功效评价等“一站式”、“全流程”的检测、咨询及申报服务。





 立即咨询
立即咨询 留言咨询
留言咨询
 1139次
1139次 2022-08-09
2022-08-09














